クロマトグラフィーの基本原理
クロマトグラフィーとは、固定相(stationary phase)と移動相(mobile phase)への分配の違いを利用して、混合物を分離する分析法です。
🏃 旅人のたとえで覚える!
カラムの中を進む成分を「旅人」、固定相を「途中にある休憩所」と想像してください。
- 休憩所が大好きな旅人(固定相に引きつけられやすい)→ 何度も立ち寄って長居する → ゴール到着が遅い=遅く溶出
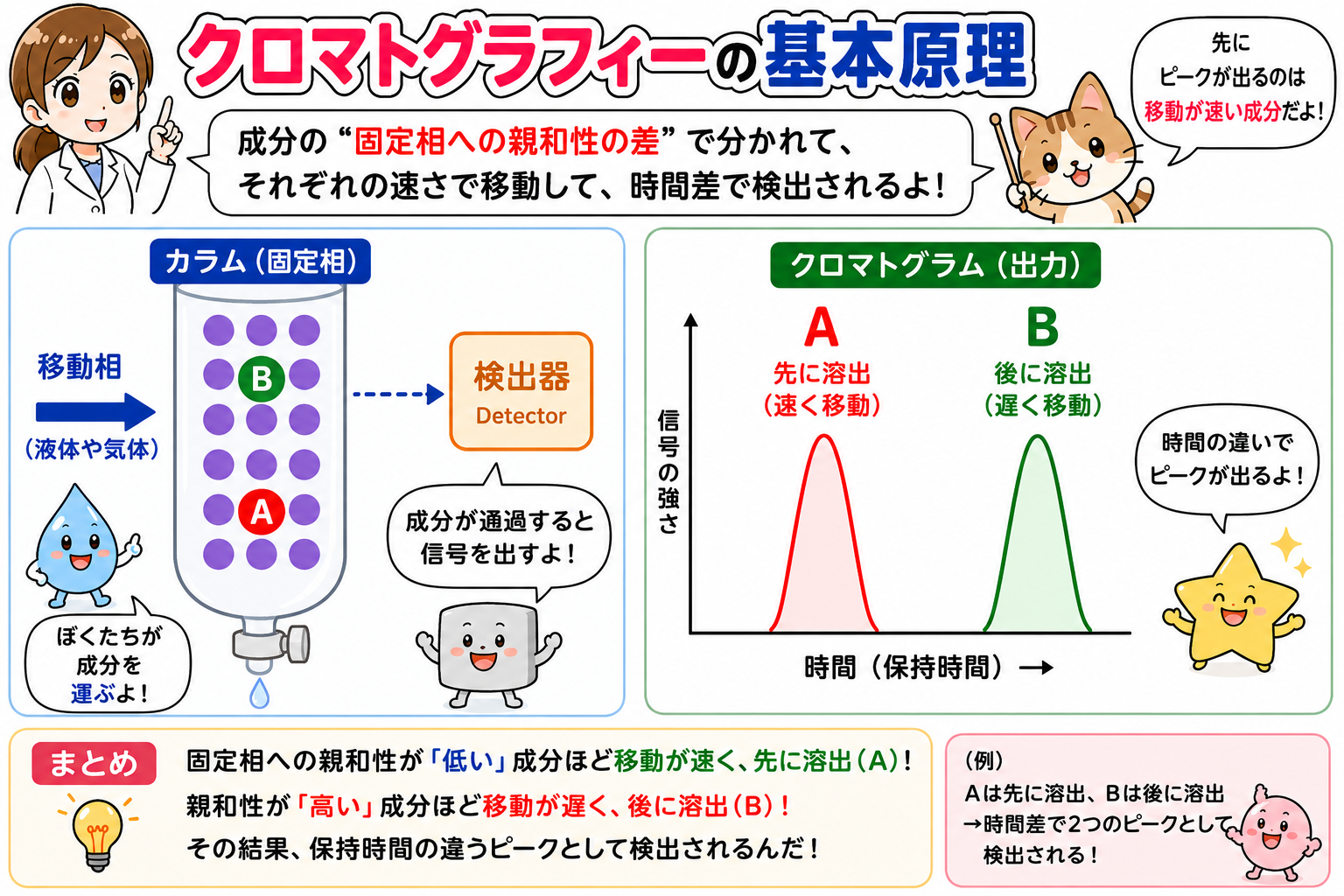
- 休憩所が嫌いな旅人(固定相に引きつけられにくい)→ 素通りしてどんどん進む → ゴール到着が早い=速く溶出
クロマトグラフィーの用語(国試必須)
| 用語 | 意味 |
|---|---|
| 保持時間(tR) | 試料注入から検出器でピークが現れるまでの時間 |
| 死時間(t0) | 固定相に保持されないピークの保持時間(カラムを素通りする成分) |
| 分離度(Rs) | 2つのピークがどれだけ分離しているかの指標。Rs ≥ 1.5で完全分離 |
| 理論段数(N) | カラム性能の指標。大きいほど分離能が高い |
| テーリング | ピークが非対称に尾を引く現象。固定相の不均一性が原因 |
① 分離モードの種類
クロマトグラフィーは分離の原理によって4種類に大別されます。
⚠️ サイズ排除(ゲル濾過)は逆! 大きい分子はゲルの細孔に入れないため先に溶出し、小さい分子は細孔に入るため遅く溶出します。
② HPLC(高速液体クロマトグラフィー)★最頻出
HPLCは移動相として液体を使用するクロマトグラフィーです。医薬品の品質試験・定量分析で最も広く使われます。
逆相 vs 順相(超頻出)
国試の鉄則:逆相HPLCは「極性が低い(疎水性)ほど保持が強く、後に溶出」
③ 薄層クロマトグラフィー(TLC)
TLCは固定相(シリカゲル等)を塗布したプレートに試料を点着し、移動相(展開溶媒)で展開する方法です。
Rf値(国試頻出計算)
$$R_f = \frac{\text{試料の移動距離}}{\text{溶媒前線の移動距離}}$$
| Rf値の意味 | 内容 |
|---|---|
| 0 ≤ Rf ≤ 1 | 0(固定相に強く保持)〜1(素通り)の間 |
| Rf値 大きい | 固定相との親和性が弱い(順相では無極性化合物) |
| 同じRf値 | 同一化合物の可能性(≠確定。他の条件でも確認) |
| 温度・溶媒で変化 | 条件を統一しないとRf値は比較できない |
⚠️ 試験での注意:TLCは吸着クロマトグラフィー(順相)が基本! 極性が大きい化合物ほどRf値が小さくなります。
④ ガスクロマトグラフィー(GC)
GCは**移動相として不活性ガス(ヘリウム・窒素・水素)**を使用します。試料は気化できることが条件です。
| 項目 | 内容 |
|---|---|
| 対象物質 | 揮発性のある化合物。沸点が低いほど分析しやすい |
| 分離原理 | 分配(固定液相への溶解度の差) |
| 特徴 | 高分解能・高感度。医薬品の残留溶媒試験(日局)に使用 |
| キャリアガス | He(ヘリウム)、N₂、H₂。不活性・試料と反応しない |
| 検出器 | FID(水素炎イオン化検出器)★最多 / TCD・ECD・MS |
GCは揮発性が必須条件! 揮発しない・熱分解しやすい化合物には液体クロマトグラフィー(HPLC)を使う。
⑤ 検出器の種類と特徴
| 検出器 | 原理 | 対象化合物 | 感度・特徴 | 国試ポイント |
|---|---|---|---|---|
| UV検出器 | UV光の吸収(254nm・280nm) | 芳香環・不飽和結合を持つ物質 | 高感度・汎用。HPLCで最も多く使われる | DAD(ダイオードアレイ検出器)は全波長を同時測定★ |
| 蛍光検出器(FLD) | 励起光を当て、発する蛍光を測定 | 蛍光性物質・誘導体化後の物質 | UV検出器より高感度・高選択性 | アミノ酸・ビタミン・生体試料の微量分析 |
| RI検出器(示差屈折率) | 移動相との屈折率の差を測定 | ほぼ全物質(汎用) | 感度は低め。グラジエント溶出には使えない | UV吸収がない物質(糖質・高分子)に使う |
| MS(質量分析) | 質量電荷比(m/z)を測定 | ほぼ全物質(構造決定も可) | 感度・選択性ともに最高 | 構造未知の代謝物・不純物の同定。LC-MS・GC-MS |
⑥ その他のクロマトグラフィー
| 種類 | 原理 | 用途・特徴 |
|---|---|---|
| アフィニティー | 抗原-抗体・酵素-基質の特異的結合 | タンパク質・抗体医薬の精製。選択性が最も高い |
| イオン交換 | 荷電基への静電的引力 | アミノ酸・核酸の分析。陽イオン交換・陰イオン交換 |
| サイズ排除(GFC/GPC) | 分子サイズの差(ゲル細孔への出入り) | 大きい分子が先に溶出★。高分子量体分析 |
| 超臨界流体(SFC) | CO₂超臨界流体を移動相に使用 | 光学異性体分離・キラル分析 |
| キャピラリー電気泳動(CE) | 電荷・サイズの差による電気泳動 | アミノ酸・核酸・不純物分析。分離効率が非常に高い |
国試頻出まとめ
絶対に覚える6ポイント
| # | ポイント | 内容 |
|---|---|---|
| 1 | 逆相HPLCの溶出順序 | 極性↑ → 先に溶出、無極性↑ → 後に溶出 |
| 2 | サイズ排除の溶出順序 | 大きい分子 → 先に溶出(細孔に入れない) |
| 3 | GCの前提条件 | 揮発性が必要。不揮発性物質にはHPLC |
| 4 | Rf値の範囲 | 0〜1(0=完全保持、1=素通り) |
| 5 | UV検出器の弱点 | UV吸収がない物質(糖質等)には不向き → RI検出器 |
| 6 | 分離度Rs | Rs ≥ 1.5 で完全分離。Rs < 1.0 は分離不十分 |
日本薬局方(JP)でのクロマトグラフィーの位置づけ
| 分析法 | 日局での主な用途 |
|---|---|
| HPLC | 定量・純度試験(含量試験・不純物試験)。最も多用 |
| GC | 残留溶媒試験。揮発性不純物の確認 |
| TLC | 確認試験(同定)・純度試験(迅速・簡便) |
| イオン交換 | 無機イオン・アミノ酸の分析 |
製造工程で使用した有機溶媒の残留を確認するのが「残留溶媒試験」 → GCが使われる!
